Soal SBMPTN 2018 Kimia nomor 39
Produk oksidasi senyawa di atas adalah ....
|
(A) |
|
|
(B) |
|
|
(C) |
✔ |
|
(D) |
|
|
(E) |
|
Pembahasan soal SIMAK UI 2019 Kimia nomor 39
gambar di soal adalah gambar alkohol sekunder, yaitu senyawa OH terikat di atom C no 2, yang terikat dengan dua atom C lain CH3-CH(OH)-CH3 , maka oksidasi alkohol sekunder menghasilkan senyawa keton CH3-C(O)-CH3
yang merupakan senyawa keton adalah  2-propanon
2-propanon
Soal SBMPTN 2018 Kimia nomor 40
Suatu senyawa yang terbentuk antara satu
atom P (nomor atom 15) dan tiga atom Br (nomor atom 35) mempunyai struktur
Lewis sebagai berikut.
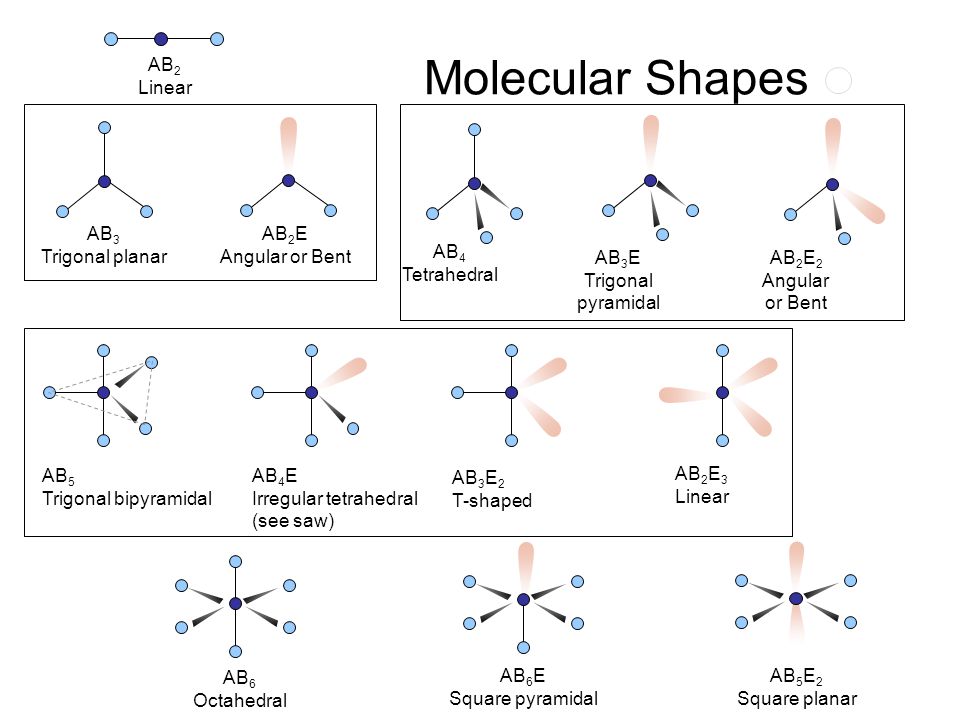
Bentuk dan kepolaran molekul tersebut adalah ....
(B) huruf T dan polar ✔
(C) tetrahedral dan nonpolar
(D) piramida segitiga dan polar
(E) planar segitiga dan polar
Pembahasan s
yang sesuai dengan soal adalah bentuk T, dan polar, karena P dan Br di bagian bawah bersifat polar
Jawabannya B
Soal SBMPTN 2018 Kimia nomor 41
Persentase massa atom karbon (Ar = 12) dalam aspirin adalah 60%.
Jika tetapan Avogadro = 6,0 × 1023, jumlah atom karbon yang terdapat dalam 3,6
g aspirin adalah ....
(B) 2,4 × 1022
(C) 4,8 × 1022
(D) 5,4 × 1022
(E) 1,08 × 1023
Pembahasan Soal SBMPTN 2018 Kimia nomor 41
ditanya jumlah atom karbon
cari mol karbon
mol C = masa C / Mr C = 60% dari 3,6 gram aspirin / 12 = 0,216 / 12 = 0,018
jumlah atom C = mol C x bilangan Avogadro = 1,08 x 1022
Jawabannya A
Soal SBMPTN 2018 Kimia nomor 42
Logam nikel (Ar = 59) bereaksi dengan gas karbon monoksida (Mr = 28) pada suhu 130 °C menurut reaksi berikut.\hspace {1cm} Ni(s) + 4CO(g) → Ni(CO)4(g)
Jika 252 g gas CO direaksikan dengan 118 g logam Ni, massa gas tetrakarbonilnikel (Mr = 171) yang dihasilkan adalah ....
(A) 430 gram
(B) 427 gram
(C) 342 gram ✔
(D) 280 gram
(E) 171 gram
Pembahasan Soal SBMPTN 2018 Kimia nomor 42
Ni(s) + 4CO(g) → Ni(CO)4(g)mol Ni(CO)4 = mol Ni = 118 / 59 = 2 mol
masa Ni(CO)4 = 2 mol x 171 = 342 gram
Jawabannya C
5. Gas metanol dapat dibuat dengan mereaksikan gas karbon monoksida dan gas
hidrogen menurut reaksi berikut.
\hspace {1cm} CO(g) + 2H2(g) → CH3OH(g)
Gas hasil reaksi tersebut pada V dan T tetap
memberikan tekanan 6 atm. Jika kedua pereaksi habis bereaksi, tekanan total gas
sebelum reaksi adalah ....
(B) 12 atm
(C) 18 atm ✔
(D) 24 atm
(E) 30 atm
Pembahasan
CO(g) + 2H2(g) → CH3OH(g)P CH3OH = 6 atm
|
CO |
2H2 |
CH3OH |
|
|
AWAL |
x |
2x |
0 |
|
REAKSI |
x |
2x |
x |
|
SETIMBANG |
0 |
0 |
x |
P CH3OH = 6 atm = x = mol CH3OH
P CO = x = 6 atm
P 2H2 = 2x = 12 atm
P total = 18 atm
Jawabannya C
6. Data nilai energi ikatan rata-rata diketahui
sebagai berikut:
|
Ikatan |
Energi Ikatan (kJ mol-1) |
|
C-H |
410 |
|
Br-Br |
193 |
|
C-Br |
267 |
|
H-Br |
363 |
CH3Br(g) + Br2(g) → CH2Br2(g) + HBr(g)
Nilai entalpi reaksi di atas adalah ....
(A) +27 kJ mol-1(B) -27 kJ mol-1 ✔
(C) +54 kJ mol-1
(D) -54 kJ mol-1
(E) +81 kJ mol-1
Pembahasan
CH3Br(g) + Br2(g) → CH2Br2(g) + HBr(g)entalpi = selisih energi di akhir reaksi dengan awal reaksi
entalpi = total energi akhir reaksi - total energi awal reaksi
ketika diawal terjadi pemutusan ikatan reaktan dan melepas energi, lalu energi tersebut dipakai untuk membentuk ikatan baru yaitu produk, jika energi yang dihasilkan di awal berlebih (hasil negatif), maka energi dikelurkan ke sistem, reaksi disebut eksoterm, sebaliknya jika energi kurang (hasil positif), reaksi akan mengambil energi dari sistem, disebut reaksi endoterm.
entalpi = energi ikatan yang dipakai di akhir - energi ikatan yang dipakai di awal
entalpi = [3(C-H) + (C-Br) + Br-Br] - [ 2(C-H) + 2(C-Br) + (H-Br) ]
entalpi = [3(410) + 267 + 193 ] - [2(410) + 2(267) + 363] kJ mol-1
entalpi = -27 kJ mol-1
Jawabannya B
7. Ion manganat (V) dapat terdisproporsionasi
sempurna menjadi ion manganat (VI) dan mangan (IV) oksida menurut reaksi (belum
setara) berikut.
2MnO_{4}^{3-}43− (aq) + H2O(l) → MnO_{4}^{2-}42− (aq)
+ MnO2(s) + 2OH-(aq)
jika 200 mL larutan manganat (V) 0,5 M bereaksi secara sempurna, jumlah mmol elektron yang terlibat adalah ....
(A) 200(B) 100
(C) 75
(D) 50 ✔
(E) 25
Pembahasan
Di soal : bereaksi sempurnaSetarakan reaksi menjadi :
2MnO_{4}^{3-}43− (aq) + H2O(l) → MnO_{4}^{2-}42− (aq) + MnO2(s) + 2OH-(aq)
2MnO43– + 2H2O → MnO2 + 4OH– + MnO42–
Disproporsionasi
2MnO_{4}^{3-}43− (V) → MnO_{4}^{2-}42− (VI) + e
2MnO_{4}^{3-}43− (V) → MnO2 (IV) + e
jumlah mol elektron terlibat = mol zat . jumlah elektron terlibat/jumlah zat
= 100 mmol . 1/2 = 50 mmol
Jawabannya D
8. Pada wadah katoda suatu sel Volta terdapat beberapa kation dengan
potensial reduksi standar (E°) sebagai berikut:
|
Ag+ + e- |
→ |
Ag |
E° = +0,80 V |
|
Fe2+ + 2e- |
→ |
Fe |
E° = -0,41 V |
|
Cr3+ + 3e- |
→ |
Cr |
E° = -0,74 V |
|
Sn2+ + 2e- |
→ |
Sn |
E° = -0,14 V |
|
Cu2+ + 2e- |
→ |
Cu |
E° = +0,34 V |
Berdasarkan data tersebut, logam yang paling mudah terbentuk di katoda adalah ....
(A) Ag ✔(B) Fe
(C) Cr
(D) Sn
(E) Cu
Pembahasan
Di soal disajikan tabel potensial reduksi standard (E) arti dari E adalah energi yang diperlukan untuk mereduksi kation itu (dinamakan potensial reduksi). Semakin besar E untuk kation itu (energi yang diperlukan semakin besar) semakin sulit kation itu untuk tereduksi, semakin kecil E semakin mudah untuk tereduksi.
Karena Ag memiliki E paling besar, Ag tereduksi lebih dahulu, dan mengendap
Dengan reaksi : Ag+ + e = Ag
Jawabannya A
9. Reaksi berikut:
\hspace {1cm} 4PH3(g) → P4(g) + 6H2(g)
Mengikuti persamaan laju -\dfrac {d[PH_{3}]} {dt}dtd[PH3] = k[PH_{3}] k[PH3]
Pada suatu percobaan dalam wadah 2 L, terbentuk
0,0048 mol gas H2 per detik ketika [PH3] = 0,1 M. Tetapan laju (kk) reaksi
tersebut adalah ....
(A) 4,8 × 10-2 s-1
(B) 3,6 × 10-2 s-1
(C) 3,2 × 10-2 s-1
(D) 2,4 × 10-2 s-1
(E) 1,6 × 10-2 s-1
Pembahasan
persamaan lajuTanda – pada ini menandakan laju pengurangan PH3
atau laju pembentukan = 0,0024 M/detik
Jawabannya E
10. Gas karbon monoksida dapat dihasilkan
melalui reaksi antara karbon dan gas karbon dioksida menurut kesetimbangan
berikut:
CO2(g) + C(s) ⇌ 2CO(g)
Jika dalam wadah 10 L dan suhu tertentu, campuran
0,8 mol CO2 dan serbuk karbon berlebih menghasilkan 0,6 mol gas CO.
Tetapan kesetimbangan, Kc, reaksi tersebut adalah ....
(B) 0,072
(C) 0,030
(D) 0,048
(E) 0,148
Pembahasan
11. Larutan A dibuat dengan melarutkan 4,16 gram
BaCl2 (Mr = 208) ke dalam 2 kg air. Barium klorida terdisosiasi
sempurna dalam air. Larutan B dibuat dengan melarutkan 15 gram zat organik
nonelektrolit ke dalam 1 kg air. Pada tekanan yang sama,
ΔTb larutan B = 2ΔTb larutan
A. Massa molekul relatif zat organik tersebut adalah ....
(B) 250 ✔
(C) 400
(D) 700
(E) 1.400
Pembahasan
nBaCl2= 4,16/208
molality BaCl2= nBaCl2 / massa pelarut = 0,02/2kg = 0,01 mol/kg
tetapan van't hoff buat BaCl2 = 3 (terioniasai sempurna)
tetapan van't hoff buat B = 1 (nonelektrolit)
ΔTb larutan B = 2ΔTb larutan A
molality B . Kb . i = 2 x (molality BaCl2 . Kb . i)
molality B x 1 = 2 x (0,01 mol/kg x 3)
molality B = 0,06 mol/kg
mol B / 1 kg = 0,06 mol / kg
mol B = 0,06 mol
Mr B = massa B / mol B = 15 gram / 0,06 mol = 1500/6 gram/mol = 250 gram/mol
Jawabannya B
12. Jika 100 mL larutan NaOH 0,5 M direaksikan
dengan 200 mL larutan aspirin (asam asetilsalisilat) 0,1 M dengan Ka = 3 ×
10-4, pH akhir larutan adalah ....
(C) 11 (D) 12 (E) 13
Pembahasan
13.
Berdasarkan reaksi berikut:
CH33OH(aq) + C22H33O_{2}^{-}2−(aq) \rightleftharpoons⇌ HC22H33O22(aq) +
CH33O-(aq)
HC22H33O22(aq) + CO_{3}^{2-}32−(aq) \rightleftharpoons⇌ HCO_{3}^{-}3−(aq) +
C22H33O_{2}^{-}2−(aq)
C66H55NH_{3}^{+}3+(aq) + OH-(aq) \rightleftharpoons⇌ C66H55NH22(aq) +
H22O(l)
Yang bukan merupakan pasangan asam-basa
konjugasi adalah ....
(B) HC22H33O22 dan HCO_{3}^{-}3−
(C) C66H55NH22 dan C66H55NH_{3}^{+}3+
(D) C22H33O_{2}^{-}2− dan HC22H33O22
(E) HCO_{3}^{-}3− dan CO_{3}^{2-}32−
Pembahasan
 Senyawa di atas yang bersifat optis aktif adalah
....
Senyawa di atas yang bersifat optis aktif adalah
....
(C) 1 dan 3 (D) 2 dan 4 (E) 4
Pembahasan
15.
Kurva di atas menyajikan data energi ionisasi 5
unsur golongan utama. Unsur yang terletak pada golongan yang sama dalam tabel
periodik adalah ....
(C) 2 dan 3 (D) 2 dan 4 (E) 2 dan 5
Pembahasan




Tidak ada komentar:
Posting Komentar
Catatan: Hanya anggota dari blog ini yang dapat mengirim komentar.